Autores
Raimundo Gerônimo da Silva Júnior, Laura Carolina López Claro, Aloísio Souza Felipe da Silva, Cleto Dantas Nogueira, Emilio Augusto Campos Pereira de Assis, Evandro Sobroza de Mello, Igor Campos da Silva.
1. Espécime e macroscopia:
Como regra geral os espécimes cirúrgicos de apêndice cecal são produtos de apendicectomias para doenças inflamatórias e menos comumente para tumores. Muitas vezes, os espécimes de apêndice cecal acompanham peças mais complexas, como colectomias ou cirurgias ginecológicas.
1.1. Macroscopia e representação histológica:
Os tipos de representação histológica dependem da indicação da apendicectomia e dos achados macroscópicos.
A representação padrão, para casos de apêndice sem lesões macroscópicas ou apendicite, deve incluir:
- Um corte da base (que pode ser a margem transversal pintada com nanquim;
- Um corte transversal central;
- As duas metades da ponta do apêndice em corte longitudinal.
A margem proximal transversal deve ser colocada em cassete separado caso seja encontrado um tumor ao exame macroscópico.
É importante realizar o exame macroscópico com a peça bem fixada, especialmente nos casos de apendicectomia por tumor.
Casos específicos:
- Pode ser necessário aumentar o número de cortes (por vezes todo o apêndice) em casos de dissociação clínico-patológica (clínica de apendicite e macroscopia sem lesões) ou em pacientes acima de 50 anos, nos quais há mais chances de neoplasia incidental.
- Para lesões tumorais: A margem proximal deve ser incluída separadamente, a superfície serosa deve ser pintada e deve-se selecionar vários cortes representativos do tumor e incluir quaisquer linfonodos identificados.
- Para neoplasia mucinosa, nas quais o apêndice está frequentemente dilatado e preenchido por mucina, a representação deve ser abundante, por vezes com inclusão total do apêndice, a fim de se demonstrar eventuais perfurações e presença de mucina ou células neoplásicas na superfície serosa.
2. Doenças inflamatórias e não neoplásicas:
2.1. Apendicite aguda:
Definição: Inflamação aguda do apêndice cecal não atribuível a outra doença subjacente.
Etiologia: Obstrução luminal associada a supercrescimento e infecção bacteriana. As principais causas de obstrução são fecalitos, mas também tumores, parasitas e hiperplasia linfoide. Outras causas são mais raras como divertículos, trauma, ou doenças vasculares.
Achados macroscópicos:
- O apêndice pode estar normal em casos de inflamação seja inicial e limitada. – A Inflamação frequentemente acomete apenas um segmento do órgão, e a correlação macro e microscópica pode ser variável.
- Edema e eritema precedem a fase de exsudato superficial purulento ou fibrinoso.
- Aos cortes pode ser observada perda de estratificação da parede e abscessos. A parede pode estar necrótica (gangrena) ou perfurada.
Achados histopatológicos:
- Inflamação aguda com predomínio de neutrófilos, envolvendo algumas ou todas as camadas do apêndice, especialmente a muscular própria (achado mais específico).
- A inflamação pode ser focal, flegmonosa (toda a parede) ou gangrenosa (com necrose e por vezes perfuração).
- Nas fases iniciais, pode haver apenas erosão da mucosa e abscessos de cripta dispersos. A inflamação se estende para lâmina própria com exsudato.
- A presença apenas de periapendicite (serosite aguda) deve ser reconhecida pois sugere causa extra-apendicular, geralmente ginecológica.
Agentes específicos: Observar eventuais inclusões virais (ex.: citomegalovírus, sarampo) ou parasitas (Enterobius vermicularis) associados à clínica de apendicite.
2.2. Apendicite granulomatosa:
Definição: Inflamação granulomatosa do apêndice.
Etiologia: Geralmente secundária, associada a infecções (Yersinia, tuberculose, fungos e parasitas) ou não infecciosas como doença de Crohn, sarcoidose ou apendicite intervalar (ver tópico abaixo). Raramente idiopática.
Achados macroscópicos:
- Não específicos, podem ser semelhantes aos da apendicite aguda.
- Espessamento da parede.
Achados histopatológicos: Inflamação granulomatosa com ou sem necrose central, associada ou não a inflamação aguda, erosões, úlceras, fissuras ou hiperplasia linfóide.
2.3. Apendicite intervalar:
Definição: Conjunto de achados patológicos encontrados em produtos de apendicectomia cuja ressecção foi retardada por tratamento clínico prévio (antibióticos e/ou drenagem).
Etiologia: Tratamento clínico conservador de apendicite aguda complicada.
Achados macroscópicos: Não específicos, podendo incluir aderências e espessamento da parede.
Achados histopatológicos:
- Inflamação granulomatosa e xantogranulomatosa com células gigantes.
- Inflamação crônica transmural com agregados linfóides e fibrose e espessamento da parede, simulando doença de Crohn.
2.4. Hiperplasia linfóide:
Definição: Reação celular benigna reversível do tecido linfóide associado a mucosa do apêndice, em resposta a estímulos inflamatórios.
Etiologia: Infecções virais (adenovírus), bacterianas, parasitárias (giardíase), adenite mesentérica, reações de hipersensibilidade e distúrbios imunes.
Achados macroscópicos: Apêndice normal ou com eventual espessamento da parede e redução luminal.
Achados histopatológicos: Hiperplasia acentuada de folículos linfóides, com agregados por vezes maiores que 2,0 mm, sem associação com apendicite aguda.
2.5. Divertículos/diverticulose:
Definição: Lesões saculares (congênitas ou adquiridas) na parede do apêndice.
Etiologia:
- Formas adquiridas (mais comuns): Associadas ao aumento da pressão luminal.
- Forma congênita: Rara, geralmente lesão única na borda antimesentérica.
Achados macroscópicos: Lesões saculares pequenas (2-5 mm), mais comuns no terço distal e borda mesentérica (adquiridas).
Achados histopatológicos:
- Formas adquiridas: Bolsas de mucosa e submucosa que atravessam a parede muscular do apêndice nos pontos de fragilidade. Podem inflamar e romper, simulando neoplasia mucinosa com ruptura.
- Formas congênitas apresentam todas as camadas da parede.
2.6. Apendicopatia obliterante:
Definição: Obliteração do lúmen apendicular por proliferação fibrosa/fusocelular benigna
Etiologia: Episódios recorrentes de inflamação apendicular
Achados macroscópicos: Geralmente sem alterações macroscópicas, mais comum no terço distal.
Achados histopatológicos: Obliteração luminal por células fusiformes em fundo fibromixoide com células inflamatórias crônicas, filetes nervosos hiperplásicos, células neuroendócrinas, adipócitos e colágeno.
3. Lesões serrilhadas do apêndice cecal
- Pólipo hiperplásico subtipo microvesicular: Reservado para lesões com serrilhamento superficial que não se estende até a muscular da mucosa.
- Lesão serrilhada séssil: Lesões com serrilhamento em toda a espessura do epitélio, atingindo a base das glândulas com expansão na muscular da mucosa (em formatos de “T invertido”, “bota” ou “L”).
O termo Lesão serrilhada séssil com displasia está reservado para aquelas lesões com presença de atipias citológicas e arquiteturais, não sendo necessário classificar entre alto e baixo grau.
Na associação de lesão serrilhada séssil com áreas de Neoplasia mucinosa, deve-se caracterizá-la como tal (LAMN/HAMN).
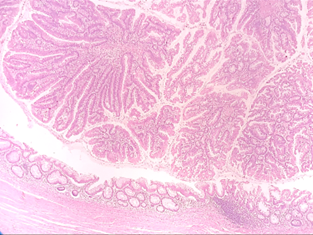
Adenoma convencional do apêndice, com características serrilhadas no lado direito da imagem.
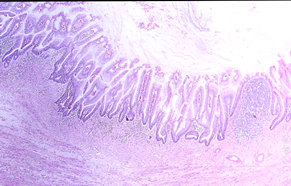
Exemplos de lesão serrilhada séssil no apêndice cecal. As características histológicas clássicas desta lesão estão presentes, mas podem ser mais sutis (devido à expansão cística do apêndice) – a presença de lâmina própria sob o epitélio neoplásico é fundamental para o diagnóstico diferencial com LAMN ou HAMN, onde o epitélio assenta-se diretamente sobre o colágeno ou a camada muscular.
4. Neoplasia mucinosa do apêndice cecal
São neoplasias epiteliais produtoras de mucina, com crescimento de padrão expansivo, sem critérios morfológicos de infiltração, mas com capacidade de disseminação mucinosa na cavidade peritoneal.
Classificam-se como Neoplasia mucinosa do apêndice cecal de baixo grau (LAMN) e Neoplasia mucinosa do apêndice cecal de alto grau (HAMN), com base em critérios histológicos. A complexidade citológica e arquitetural determina o grau histológico.
Achados macroscópicos:
Os achados macroscópicos podem variar desde aspecto normal a dilatação cística contendo muco em quantidades variáveis.
- A parede pode ser fibrosada e calcificada.
- É essencial observar áreas de perfuração ou de mucina na superfície serosa e avaliar as margens cirúrgicas (óstio e mesentérica).
- O processamento macroscópico deve ser cuidadoso para evitar a contaminação da superfície serosa com mucina.
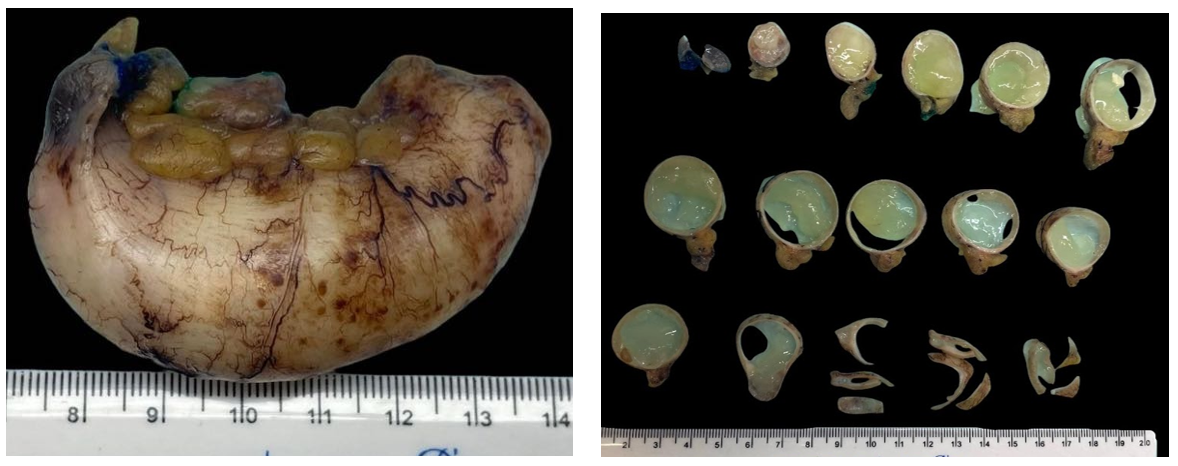
Apêndice cecal dilatado, exibindo lúmen cistificado e com abundante conteúdo mucinoso.
Achados microscópicos:
O epitélio apendicular observa-se substituído circunferencialmente por epitélio mucinoso proliferativo viloso, plano ou com serrilhamento superficial e frequente atrofia do tecido linfoide com fibrose da lâmina própria e submucosa, por vezes com focos de calcificação distrófica.
4.1. Neoplasia mucinosa do apêndice cecal de baixo grau (LAMN):
- O epitélio neoplásico está composto por células colunares ricas em mucina, com núcleo alongado, hipercromático e pseudoestratificado, sem complexidade arquitetural.
- Atividade mitótica é usualmente baixa e limitada à base do epitélio.
- Padrão de crescimento expansivo, com dissecção mural de mucina sem aspecto infiltrativo, podendo haver herniação do epitélio através da muscular própria.
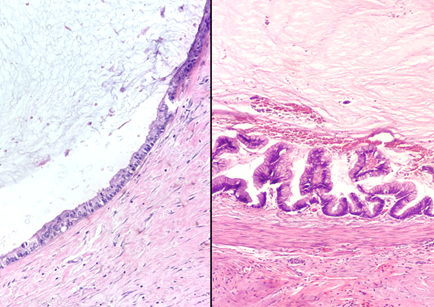
Neoplasia mucinosa de baixo grau do apêndice cecal (LAMN)
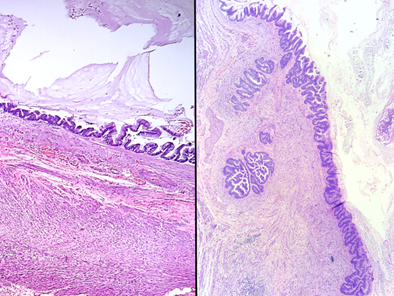
Neoplasia mucinosa do apêndice de baixo grau (LAMN, à esquerda) e de alto grau (HAMN, à direita). Repare que o epitélio da lesão assenta-se diretamente sobre o colágeno ou a camada muscular, não existe lâmina própria – um dos achados mais característicos da lesão (que também é chamado de invasão em “broad front”) e essencial para a diferenciação com as lesões serrilhadas, principal diagnóstico diferencial.
4.2. Neoplasia mucinosa do apêndice cecal de alto grau (HAMN):
- Características semelhantes à LAMN, mas com micropapilas e arranjos cribriformes.
- Perda de polaridade, estratificação verdadeira, depleção de mucina celular, atipia nuclear, hipercromasia e pleomorfismo intensos.
- Mitoses nos terços superiores da célula é frequente.
- Debris celular e focos de necrose também podem ser vistos.
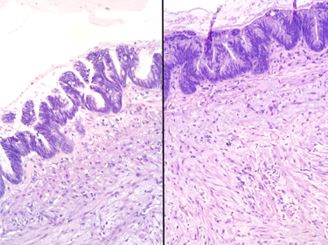
Neoplasia mucinosa de alto grau do apêndice cecal (HAMN).
Denudação da mucosa e áreas de ulceração podem ser observadas, pois quadros de apendicite aguda podem coexistir com estas neoplasias.
Essas neoplasias podem revestir divertículos do apêndice cecal, mas esse achado não deve ser confundido com carcinoma invasivo.
5. Prognóstico
- O prognóstico depende do estadiamento patológico.
- Tumores confinados ao apêndice tem um excelente prognóstico.
- Casos com ruptura e extravasamento de mucina acelular à cavidade peritoneal e órgãos adjacentes (ex.: ovário) apresentam maior risco de recidiva.
O grau histológico dessas neoplasias será discutido na tabela 1.
6. Estadiamento
- Segundo o AJCC, as neoplasias confinadas à mucosa, submucosa e muscular própria são estadiadas como in situ (pTis).
- Extensão à subserosa é estadiada como pT3, enquanto envolvimento da serosa é pT4a.
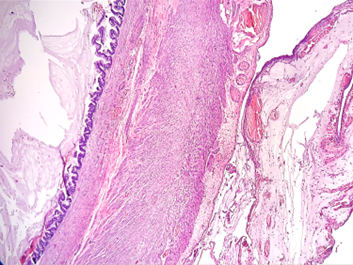
Neoplasia mucinosa de baixo grau do apêndice cecal (LAMN), com presença de mucina acelular na superfície serosa. Mesmo a mucina sendo acelular, este caso já é classificado como pT4a.
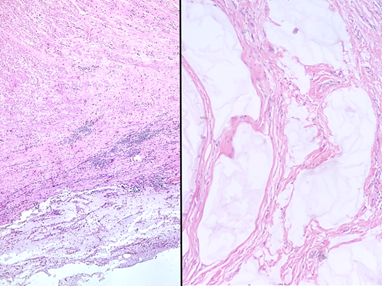
Mucina acelular na serosa do apêndice (pT4a) e no epíplon (pM1a). Muitas vezes há fibroblastos, vasos e inflamação no meio da mucina – como não há células neoplásicas, a mucina é considerada como acelular, um indicador de melhor prognóstico mesmo quando há um quadro de “pseudomixoma peritonei”
7. Adenocarcinoma do apêndice cecal
Neoplasia epitelial maligna e invasiva do apêndice cecal.
Subtipos histológicos:
A Organização Mundial da Saúde reconhece os subtipos: Adenocarcinoma convencional (SOE), Adenocarcinoma mucinoso, Adenocarcinoma com células em anel de sinete e Carcinoma indiferenciado.
Achados morfológicos:
À macroscopia a neoplasia pode se apresentar como polipoide, ulcerada ou úlcero-infiltrativo, podendo causar oclusão luminal.
7.1 Adenocarcinoma mucinoso:
É o subtipo mais comum. Por definição, contém >50% de mucina extracelular e frequentemente está acompanhado de glândulas e pequenos grupamentos celulares. Embora infrequente, arranjos cribriformes podem ser observados.
As atipias citológicas podem variar de discretas a intensas. A chave para o diagnóstico é o padrão infiltrativo, não expansivo.
A graduação histológica destes tumores acompanha a usada para lesões mucinosas:
| Grau tumoral | Características histológicas |
| Grau 1 | Neoplasia mucinosa de baixo grau (LAMN) |
| Grau 2 |
|
| Grau 3 |
|
Tabela 1. Graduação histológica de neoplasias mucinosas e adenocarcinoma mucinoso.
7.2. Adenocarcinoma convencional/tipo intestinal:
Semelhante ao carcinoma colorretal, com glândulas irregulares/anguladas infiltrativas compostas por células colunares altas com citologia de baixo e alto grau, em meio a um estroma desmoplásico.
Associado frequentemente a adenoma tubular/tubuloviloso ou uma lesão precursora serrilhada.
Brotamentos tumorais também podem ser observados e devem ser relatados.
Ao contrário do adenocarcinoma mucinoso, raramente resulta em pseudomixoma peritoneal.
Graduação histológica:
- OMS: Sistema de classificação de dois níveis: baixo grau (bem e moderadamente diferenciados) e alto grau (pouco diferenciados),
- Colégio Americano de Patologia: Sistema baseado na porcentagem de estruturas glandulares:
- Bem diferenciado (G1, >95% de formação de glândulas).
- Moderadamente diferenciado (G2, 50–95% de formação de glândulas).
- Pouco diferenciado (G3, <50% de formação de glândulas).
7.3. Adenocarcinoma com células em anel de sinete:
- Por definição, >50% das células apresentam morfologia de anel de sinete.
- Infiltração da parede ocorre por células isoladas, em pequenos grupos ou acompanhando lagos de mucina transmural.
- Comportamento agressivo, frequentemente associado a apresentação clínica de apendicite aguda.
Diagnóstico diferencial:
Neoplasias mucinosas de alto e baixo grau (LAMN/HAMN) são os diagnósticos diferenciais mais importantes, principalmente para os adenocarcinomas mucinosos, sendo necessário reconhecer o padrão infiltrativo com pelo menos um foco de invasão verdadeira no adenocarcinoma. O aspecto destrutivo, com presença de glândulas irregulares e infiltrativas dentro de um estroma desmoplásico celular caracteriza o diagnóstico de adenocarcinoma mucinoso.
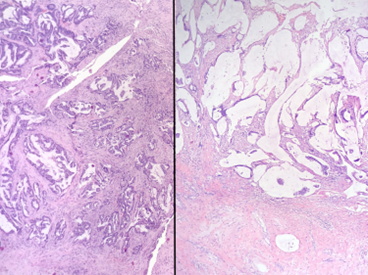
Dois exemplos de adenocarcinoma do apêndice – características de invasão estromal, nestes casos, são bastante evidentes e diferenciam esta neoplasia da LAMN e da HAMN, onde a invasão é do tipo “broad front”.
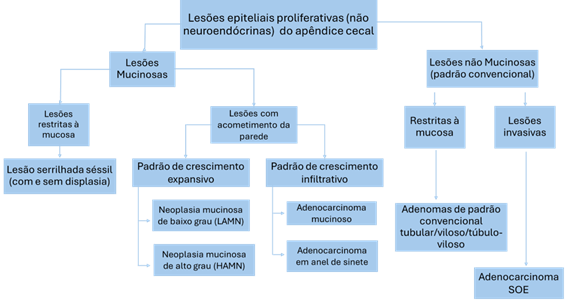
Fluxograma de lesões proliferativas epiteliais.
8. Adenocarcinoma de células caliciformes (Goblet cell adenocarcinoma)
São tumores compostos por células caliciformes semelhantes às do trato intestinal, uma quantidade variável de células endócrinas e células Paneth símiles, dispostas em túbulos ou grupamentos. Por definição, estes tumores devem mostrar pelo menos um componente de carcinoma de células caliciformes de baixo grau (Grau 1).
Baixo grau:
- Caracterizado por formações tubulares compostas principalmente por células caliciformes e componentes variáveis de células neuroendócrinas e de células de Paneth símile, estas últimas com citoplasma eosinofílico e granular.
- Os três componentes apresentam atipias nucleares discretas e baixo índice mitótico.
- Geralmente há comprometimento circunferencial em meio a um estroma pouco desmoplásico.
Alto grau:
- Caracterizado pela perda dos agrupamentos celulares e túbulos bem formados.
- Presença de células isoladas (mucinosas ou não mucinosas), infiltrativas, associadas a túbulos anastomosantes, arranjos cribriformes e grandes agregados de células em anel de sinete ou de células caliciformes.
- Reação desmoplásica é intensa e a taxa de mitoses é alta.
Diagnóstico diferencial:
O principal diagnóstico diferencial é o adenocarcinoma em anel de sinete, principalmente em tumores de alto grau com importante componente dessa morfologia.
Terminologia:
Não é mais recomendado o uso do termo Carcinoide de células caliciformes (Goblet cell carcinoide), pois hoje é bem reconhecido que o componente neuroendócrino desta neoplasia é menor quando comparado ao das células mucinosas (caliciformes).
