Autores
Raimundo Gerônimo da Silva Júnior, Laura Carolina López Claro, Aloísio Souza Felipe da Silva, Cleto Dantas Nogueira, Emilio Augusto Campos Pereira de Assis, Evandro Sobroza de Mello, Igor Campos da Silva.
1. Panorama geral:
As Neoplasias neuroendócrinas abrangem um amplo e heterogêneo grupo de neoplasias epiteliais que podem surgir em quase qualquer sítio anatômico e, apesar de apresentarem algumas características em comum (presença de grânulos neurossecretores, aspectos histológicos e perfil imuno-histoquímico), também apresentam variações clínicas e biológicas.
O padrão de distribuição ao longo do trato gastrointestinal (TGI) geralmente reflete o tipo de célula progenitora, e o sítio anatômico de origem é um importante preditor do comportamento clínico.
Devido às semelhanças específicas, e independente do local em relação à histologia, histoquímica e perfil imuno-histoquímico, os tumores neuroendócrinos do trato digestivo têm sido tradicionalmente subdivididos em tumores do TGI anterior, médio e posterior.
2. Amostragem endoscópica:
A coleta e o manuseio adequados de amostras de tecido durante a endoscopia são fundamentais no diagnóstico de patologias do sistema digestivo.
- São necessários de 6 a 8 fragmentos por lesão para garantir material suficiente (inclusive para a obtenção do número de células necessárias para avaliação de ki-67).
- A avaliação de áreas normais próximas é recomendada para comparação histológica e diagnóstico de possíveis condições predisponentes (por ex. Gastrite autoimune).
- As amostras devem ser acondicionadas em frascos separados, devidamente identificados, e fixados em formalina tamponada a 10%.
- É essencial que as amostras sejam acompanhadas de requisição com informações clínicas detalhadas, incluindo a história da doença atual e achados endoscópicos.
3. Classificação das neoplasias neuroendócrinas
A classificação das neoplasias neuroendócrinas pela Organização Mundial da Saúde (OMS) em 2017 trouxe uma abordagem padronizada e mais precisa para categorizar essas lesões, destacando a importância da morfologia como o critério principal. A seguir, os principais aspectos da classificação são detalhados:
| Terminologia | Diferenciação | Índice mitótico (2 mm²) | Índice de Ki-67 |
TNE
|
Bem diferenciado | <2
2-20 >20 |
<3%
3-20% >20% |
CNE
|
Pouco diferenciado | >20
>20 |
>20% >20%
|
| MINEN | Bem ou pouco diferenciados | Variável | Variável |
Tabela 1. Classificação das neoplasias neuroendócrinas segundo a última publicação da Organização Mundial da saúde.
3.1 Neoplasias Neuroendócrinas Bem Diferenciadas (Tumores Neuroendócrinos)
As neoplasias neuroendócrinas bem diferenciadas incluem tumores primários ou metastáticos que compartilham características histológicas e moleculares específicas. São tumores de comportamento biológico mais favorável em comparação aos carcinomas neuroendócrinos pouco diferenciados.
Achados microscópicos
Arquitetura com padrões característicos, como ninhos, trabéculas, cordões ou rosetas.
Células uniformes, geralmente pequenas e médias, com núcleo arredondado e citoplasma escasso. A cromatina tem aspecto em “sal e pimenta”.
Grau Histológico
A classificação histológica dos Tumores Neuroendócrinos (TNE) baseia-se na taxa mitótica e no índice Ki-67, sendo esses critérios fundamentais para a determinação do grau, que orienta o manejo clínico e auxilia na avaliação prognóstica.
Taxa Mitótica
Deve ser relatada como o número de mitoses por 2 mm².
A contagem deve incluir pelo menos 10 mm² na área de maior atividade mitótica.
Apenas figuras mitóticas claramente identificáveis devem ser consideradas. Núcleos apoptóticos, hipercromáticos ou cariorréticos não devem ser contados.
Ajuste por Campo: Devido às variações no tamanho do campo de alta potência (CGA), o número de campos para atingir 2 mm² deve ser ajustado de acordo com o microscópio utilizado.
Índice Ki-67
Relatado como a porcentagem de células tumorais positivas na área de maior marcação nuclear (“hot spot”).
A avaliação deve incluir pelo menos 500 células tumorais. Se o número de células for menor, essa limitação deve ser mencionada no laudo.
Métodos automatizados podem ser usados, mas necessitam de validação para minimizar imprecisões.
O índice Ki-67 frequentemente resulta em um grau maior do que o baseado na contagem mitótica. Quando ambos os métodos são realizados, o grau final deve ser atribuído ao maior valor.
A necrose, embora não seja um critério obrigatório para a classificação dos TNEs do trato digestivo, sua presença deve ser relatada no laudo, pois pode refletir comportamento mais agressivo.
Classificação de Grau pela OMS:
Grau 1 (Baixo Grau): Taxa mitótica <2 mitoses/10 CGA. Ki-67 <3%.
Grau 2 (Intermediário): Taxa mitótica entre 2–20 mitoses/10 CGA.Ki-67 entre 3–20%.
Grau 3 (Alto Grau): Taxa mitótica >20 mitoses/10 CGA ou Ki-67 >20%.
Tumores grau 3 mantêm características morfológicas de bem diferenciados, diferenciando-se dos carcinomas pouco diferenciados.
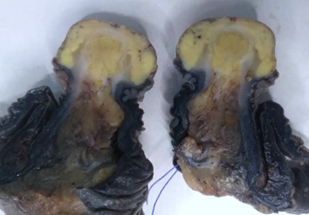
Macroscopia de Neoplasia neuroendócrina de intestino delgado. Lesão polipoide amarelo-esbranquiçada, bem delimitada, com comprometimento de mucosa e submucosa.
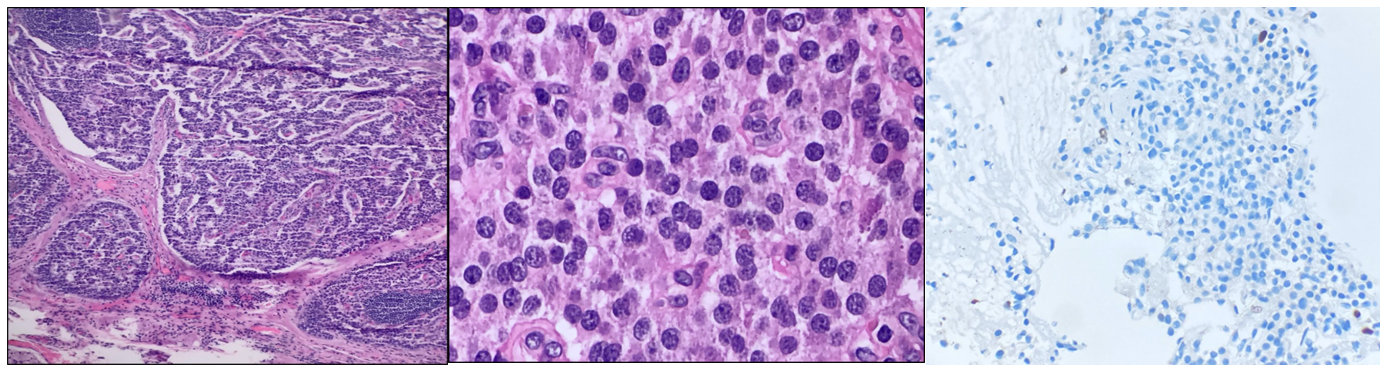
Tumor neuroendócrino, bem diferenciado. A neoplasia apresenta arranjo organoide, com escassas atipias citológicas, citoplasma eosinofílico amplo e núcleo exibindo o clássico aspecto de “sal e pimenta”. No exame imuno-histoquímico (ki67) raras células apresentam positividade (<2%).
Imuno-histoquímica
A imuno-histoquímica é uma ferramenta essencial para o diagnóstico de neoplasias neuroendócrinas, especialmente para diferenciar tumores bem diferenciados. Os marcadores recomendados incluem:
Marcadores Neuroendócrinos Gerais:
- Cromogranina A: Específico para grânulos neuroendócrinos.
- Sinaptofisina: Amplo espectro de expressão em neoplasias neuroendócrinas.
- CD56: Marcador menos específico, mas frequentemente positivo.
- INSM1: Marcador emergente com alta sensibilidade e especificidade.
Citoqueratinas:
- AE1/AE3 e CAM5.2: Essenciais para diferenciar tumores neuroendócrinos de lesões como paragangliomas e tumores glômicos, que não expressam citoqueratinas.
Marcadores Hormonais:
- Hormônios específicos: Como gastrina, insulina e glucagon. Auxiliam no diagnóstico, mas não necessariamente indicam funcionalidade clínica.
Marcadores de Sítio Primário:
- TTF-1: Sugere sítio primário pulmonar ou tireoidiano e exclui origem no trato gastrointestinal (TGI).
- CDX2: Comumente expresso em tumores do apêndice, intestino delgado e, variavelmente, em estômago e cólon.
- SATB2 e PrAP: Associados a tumores retais.
A escolha dos marcadores deve ser direcionada pelo contexto clínico e pela apresentação morfológica, complementando a análise histopatológica para um diagnóstico preciso e definição de sítio primário.
Prognóstico:
- Grau Proliferativo:
- Grau 1: Melhor prognóstico, com sobrevida em 5 anos >90% em casos localizados.
- Grau 2: Prognóstico intermediário, sobrevida em 5 anos de 60–80%.
- Grau 3: Comportamento mais agressivo, sobrevida geralmente <3 anos em casos avançados.
Observações quanto a localização:
Estômago
Os três principais tipos de tumores neuroendócrinos do estômago são:
Tipo 1:
- Associado a hipergastrinemia devido a gastrite crônica atrófica autoimune.
- A maioria dos casos é grau 1 ou 2, sendo raro um grau 3.
- Ao avaliar um tumor neuroendócrino gástrico fique atento aos achados da mucosa adjacente. Caso não haja esta representação, relate e solicite biópsias da mucosa adjacente ao TNE.
Tipo 2:
- Associado a síndrome de Zollinger-Ellison (hipergastrinemia), devido a gastrinoma duodenal ou pancreático.
Tipo 3:
- Esporádicos, com o grau variando de G1-G3, entretanto, frequentemente com maior risco de metástase e estágio do tumor.
Duodeno:
- Os TNE duodenais representam cerca de 4% dos tumores neuroendócrinos gastrointestinais.
- A maioria dos TNEs duodenais e ampulares não é funcional.
- Histologicamente, os somastostinomas apresentam padrão glandular puro, com corpos de psammoma dispersos, podendo ser confundidos com adenocarcinomas convencionais. A imuno-histoquímica é essencial para o diagnóstico diferencial.
3.2. Neoplasias Neuroendócrinas Pouco Diferenciadas (Carcinomas Neuroendócrinos)
Os carcinomas neuroendócrinos são neoplasias epiteliais altamente agressivas, caracterizadas por morfologia de alto grau, expressão variável de marcadores neuroendócrinos e, por definição, apresentam taxa mitótica >20 mitoses/10 CGA ou índice Ki-67 >20%. Histologicamente, são subdivididos em carcinomas de pequenas células e carcinomas de grandes células.
Carcinoma de Pequenas Células
- Neoplasia com padrão de crescimento em ninhos sólidos, cordões, ou arranjo difuso, frequentemente exibindo invasão destrutiva do estroma. Algumas áreas podem mostrar pseudorosetas, mas sem organização glandular verdadeira.
- Células pequenas, com núcleos hipercromáticos, de formato predominantemente redondo ou oval. A cromatina é granular fina, sem nucléolos evidentes. O citoplasma é ausente ou muito escasso.
- Alta atividade mitótica, com mitoses abundantes e presença frequente de corpos apoptóticos.
- Necrose extensa e frequente, refletindo a elevada taxa proliferativa.
- Presença de artefato de esmagamento celular, característico devido à fragilidade celular.
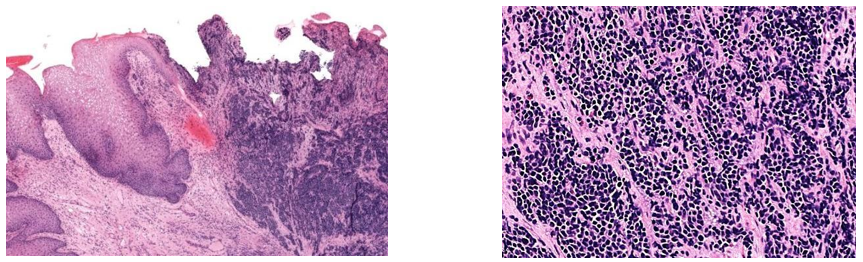
Carcinoma neuroendócrino de pequenas células anorretal. Pequenas células hipercromáticas em arranjo difuso infiltrando o estroma, com frequentes figuras de mitoses e corpos apoptóticos.
Carcinoma de Grandes Células
- Neoplasia com padrão de crescimento sólido, trabecular ou em ninhos, apresentando francos sinais de invasão destrutiva no estroma. Áreas de necrose central extensa são frequentes, e rosetas ou pseudoglandulares podem estar presentes.
- As células são maiores, com núcleos vesiculares ou hipercromáticos, cromatina granular e nucléolos frequentemente proeminentes. Relação núcleo:citoplasma diminuída, com citoplasma moderado a escasso.
- A população celular é pleomórfica, exibindo alta atipia e variação no tamanho e na forma nuclear.
- A atividade mitótica é elevada, com mitoses atípicas e numerosas, frequentemente superiores a 20 mitoses por 10 campos de grande aumento.
A necrose é geralmente extensa, frequentemente em padrão geográfico, associada à alta taxa proliferativa.
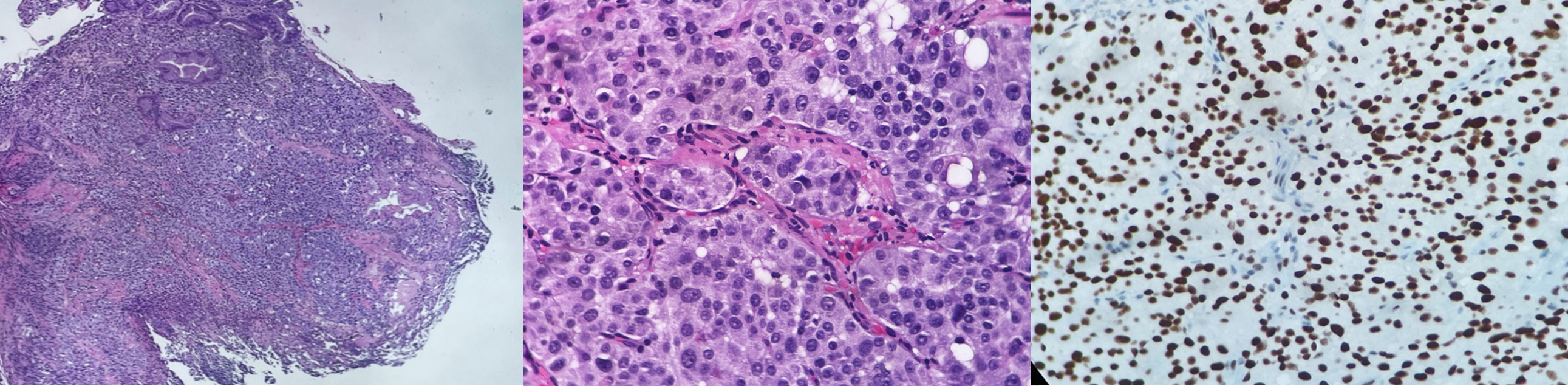
Carcinoma neuroendócrino, pouco diferenciado (G3) de grandes células. Neoplasia com francos sinais infiltrativos, atipias citológicas marcadas, pleomorfismo e presença de mitoses atípicas. No exame imuno-histoquímico, alta taxa proliferativa com Ki-67 >50%.
Imuno-Histoquímica
- Cromogranina A, sinaptofisina, CD56 e INSM1 são frequentemente expressos, mas podem ser de expressão variável.
- Ki-67: Geralmente >50%, indicando alta proliferação celular.
- Citoqueratinas (AE1/AE3, CAM5.2): Confirmam origem epitelial.
Prognóstico:
Subtipos:
Pequenas células: Prognóstico reservado, progressão rápida, frequentemente metastático ao diagnóstico.
Grandes células: Um pouco menos agressivo, mas ainda associado a alta mortalidade.
Sobrevida:
Doença localizada: Sobrevida média de 1–2 anos.
Doença avançada/metastática: Sobrevida geralmente <1 ano.
3.3. Neoplasias Mistas Neuroendócrinas e Não Neuroendócrinas (MINEN)
As Neoplasias Mistas Neuroendócrinas e Não Neuroendócrinas (MINEN) são tumores raros que apresentam dois componentes distintos: um neuroendócrino (bem ou pouco diferenciado) e um não neuroendócrino, como adenocarcinoma ou carcinoma escamoso, ambos contribuindo significativamente (≥30%) para a composição tumoral.
Achados microscópicos
Componente Neuroendócrino:
- Quando bem diferenciado, apresenta padrões típicos como ninhos, trabéculas ou rosetas, com núcleos exibindo cromatina com aspecto em “sal e pimenta”.
- Quando pouco diferenciado, exibe alta atipia nuclear, necrose extensa, e elevada taxa mitótica ou Ki-67.
Componente Não Neuroendócrino:
- Mais comumente adenocarcinoma (como no trato gastrointestinal), mas pode ser carcinoma escamoso ou outros subtipos.
- O grau de diferenciação do componente não neuroendócrino varia amplamente.
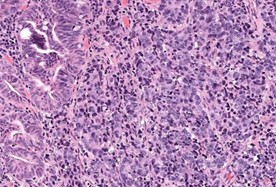
MINEN – neoplasia com componente adenocarcinomatoso (à esquerda) e neuroendócrino de grandes células.
Imuno-Histoquímica
Componente Neuroendócrino:
- Marcadores neuroendócrinos gerais: Cromogranina A, Sinaptofisina, CD56 e INSM1.
- Taxa proliferativa avaliada por Ki-67.
Componente Não Neuroendócrino:
- Citoqueratinas: AE1/AE3, CAM5.2.
- Outros marcadores específicos de linhagem (como CDX2 para adenocarcinoma de origem intestinal ou p40 para carcinoma escamoso).
Prognóstico
- O prognóstico depende do grau de diferenciação e da agressividade de ambos os componentes.
- Tumores com componente neuroendócrino pouco diferenciado têm pior prognóstico.
