Thais Heinke
Códigos de topografia
C21.0 Ânus, SOE
C21.1 Canal anal
C21.8 Lesão de reto, ânus e canal anal
I. Identificação e resumo clínico
II. Dados clínicos relevantes
II.1 Estudo citológico
- Não realizado
- Diagnóstico ___________
Data ___/___ /___
II.2 Imunodepressão/supressão
- Não
- Sim (especificar)
II.3 Estudo biomolecular (pesquisa para HPV)
- Não realizado
- Realizado (resultado) ___________
II.4 Tratamento prévio
- Não
- Sim (especificar local) ___________
III. Procedimento cirúrgico
- Biópsia incisional
- Excisão local ampla
- Ressecção abdominoperineal
- Outro (especificar) _____________
IV. Exame macroscópico
IV.1 Tamanho do espécime ___ x ___ x ___ cm
IV.2 Lesão
- Não identificável macroscopicamente
- Única
- Múltiplas (identificar margens, outras lesões e incluir separadamente)
Medidas ___ x ___ x ___ cm
Maior dimensão _____ cm
Padrão
- Ulcerada
- Plana
- Exofítica
- Outro (especificar) ________
Localização (especificar) ________
Nota: O canal anal apresenta três zonas diferentes: zona colorretal, zona de transição (se estendendo a partir da linha pectínea proximalmente situada entre a mucosa de tipo colorretal ininterrupta acima e o epitélio escamoso ininterrupto abaixo) e zona escamosa (se estendendo a partir da linha pectínea distalmente até a junção mucocutânea e destituída de apêndices cutâneos) (Figura 1). Tumores comprometendo canal anal (incluindo os três tipos de mucosa da região) e que não são observados ao exame do paciente, com tração e afastamento das nádegas, são considerados como câncer anal, enquanto tumores da pele ou da junção mucocutânea, que possam ser visualizados ao exame, com afastamento das nádegas, e estão a até 5,0 cm do ânus, são considerados cânceres perianais.
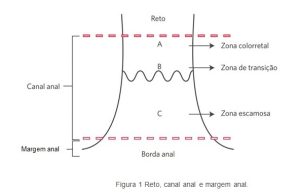
Figura 1 Reto, canal anal e margem anal.
IV.3 Linfonodos
- Não identificados macroscopicamente
- Presentes (especificar número, tamanho e localização)________
Nota: A drenagem linfática depende da localização do tumor primário; tumores acima da linha pectínea tendem a se disseminar em linfonodos anorretais, perirretais e paravertebrais, enquanto tumores abaixo da linha pectínea tendem a se disseminar em linfonodos inguinais superficiais.
IV.4 Processamento macroscópico
Além dos procedimentos de rotina, é necessário:
- Localizar a lesão ao exame macroscópico e abrir longitudinalmente o espécime sem transfixar a lesão; pintar com o corante a margem circunferencial mais próxima ao tumor, bem como as margens distal e proximal.
• Fazer cortes que incluam o tumor em toda a sua profundidade, incluindo assim a representação da margem circunferencial (sempre que possível); incluir, ainda, fragmentos representativos das margens proximal e distal.
• Assegurar-se de incluir, sempre que possível, um fragmento no qual esteja representada a transição entre a lesão e a mucosa/pele macroscopicamente íntegra.
• Representar fragmentos de mucosa adjacentes à lesão.
• Identificar as margens como distal, proximal e circunferencial, pintando-as antes de coletar as amostras desses pontos.
V. Exame microscópico
V.1 Tipo histológico (OMS/2010)
- 8070 Carcinoma espinocelular (escamocelular)
- 8077 Neoplasia intraepitelial escamosa, alto grau (anteriormente doença de Bowen)
- 8051 Carcinoma verrucoso, SOE
- 8020 Carcinoma indiferenciado, SOE
- 8140 Adenocarcinoma, SOE
- 8542 Doença de Paget, extramamária
- 8480 Adenocarcinoma mucinoso
- 8090 Carcinoma basocelular, SOE
- 8246 Carcinoma neuroendócrino
- 8041 Carcinoma neuroendócrino de pequenas células
- 8013 Carcinoma neuroendócrino de grandes células
- 8244 Carcinoma misto adenoneuroendócrino
- Outro (especificar) __________
V.2 Grau histológico
- Não determinado
- Grau 1 – Bem diferenciado
- Grau 2 – Moderadamente diferenciado
- Grau 3 – Pouco diferenciado
- Grau 4 – Indiferenciado
V.3 Profundidade de invasão
- Carcinoma in situ
- Invasão de lâmina própria
- Invasão da muscular da mucosa
- Invasão da submucosa
- Invasão do músculo esfincteriano
- Invasão de pele perianal
- Profundidade de invasão ______ mm
V.4 Invasão vascular
- Não detectada
- Detectada
- Sanguínea
- Linfática
V.5 Invasão perineural
- Não detectada
- Detectada
V.6 Margens cirúrgicas
- Livres de neoplasia invasiva, distando a mais próxima _____ cm do componente invasivo
- Comprometida(s) pelo componente invasivo; especificar a margem (quando possível) ________________
- Presença do componente in situ da lesão na margem
V.7 Mucosa adjacente (especificar) __________
VI. Diagnóstico final (exemplo)
Produto de ressecção abdominoperineal de lesão anal com linfadenectomia:
- Carcinoma espinocelular invasivo bem diferenciado (grau 1), exofítico, medindo 1,7 x 1,3 x 0,9 cm, localizado em parede anterior da região mucosa de canal anal, infiltrando a camada submucosa.
- Profundidade de infiltração neoplásica: 6,0 mm.
- Invasão angiolinfática não detectada.
- Margens de ressecção circunferencial, distal e proximal livres de comprometimento neoplásico.
- Presença de neoplasia intraepitelial escamosa de alto grau adjacente à lesão, não comprometendo as margens cirúrgicas de ressecção.
- Ausência de metástase nos linfonodos regionais dissecados (0/6).
• Estadiamento patológico: pT1 pN0 pMx; estádio I.
VII. Comentários
VII.1 Classificação TNM dos carcinomas de canal anal (AJCC 8th ed.)
T – Tumor primário
- pTx – Não disponível
- pT0 – Sem evidências de tumor primário
- pTis – Lesão intraepitelial escamosa de alto grau (carcinoma in situ, doença de Bowen, neoplasia intraepitelial anal II a III e neoplasia intraepitelial de alto grau)*
- pT1 – Tumor ≤ 2 cm em sua maior dimensão**
- pT2 – Tumor > 2 cm e ≤ 5 cm em sua maior dimensão
- pT3 – Tumor > 5 cm em sua maior dimensão
- pT4 – Tumor de qualquer tamanho com invasão de órgãos adjacentes, como vagina, uretra e bexiga (invasão direta do tecido subcutâneo, da pele perianal e dos músculos esfincterianos não qualifica o tumor como pT4)
* Nota 1: A lesão intraepitelial escamosa anal de alto grau é considerada uma lesão precursora do carcinoma anal, podendo ser identificada por citologia, anuscopia de alta resolução e/ou biópsia.
** Nota 2: Há uma recomendação do Lower Anogenital Squamous Terminology Standardization Project for HPV-associated Lesions (The CAP-ASCCP LAST Project) de que a terminologia “carcinoma espinocelular superficialmente invasivo do canal anal” [superficially invasive squamous cell carcinoma of the anal canal (SISCCA)] seja utilizada quando a neoplasia apresentar profundidade de invasão ≤ a 3,0 mm a partir da membrana basal e ≤ 7,0 mm de extensão horizontal máxima, e tiver sido feita a ressecção completa da lesão.
N – Linfonodos regionais
- pNx – Não disponíveis
- pN0 – Metástase linfonodal não observada
- pN1 – Metástase em linfonodo(s) inguinal, mesorretal, ilíaco interno ou ilíaco externo
- pN1a – Metástase em linfonodo(s) inguinal, mesorretal ou ilíaco interno
- pN1b – Metástase em linfonodo(s) ilíaco externo
- pN1c – Metástase em linfonodo(s) ilíaco externo com qualquer pN1a
M – Metástase a distância
- M0 – Ausente
- M1 – Presente
VII.2 Estádios anatômicos/grupos prognósticos
Tabela 1 Estádios anatômicos/grupos prognósticos do câncer de ânus.
| Grupo | T | N | M |
| 0 | Tis | N0 | M0 |
| I | T1 | N0 | M0 |
| IIA | T2 | N0 | M0 |
| IIB | T3 | N0 | M0 |
| IIIA | T1 | N1 | M0 |
| IIIA | T2 | N1 | M0 |
| IIIC | T3 | N1 | M0 |
| IIIB | T4 | N0 | M0 |
| IIIC | T4 | N1 | M0 |
| IV | Qualquer T | Qualquer N | M1 |
VIII. Considerações gerais
VIII.1 Tumores da pele perianal, margem anal e canal anal
Tumores originados na pele da região perianal e na margem anal (junção entre a mucosa escamosa e a pele) se comportam de maneira similar aos cânceres de outros sítios cutâneos e devem ser estadiados de acordo com os outros cânceres de pele das demais topografias.
No entanto, seguem algumas considerações gerais a respeito de algumas entidades morfológicas que podem apresentar peculiaridades da região anal:
- Doença de Bowen: é uma variante do carcinoma espinocelular in situ, raramente acomete a região perianal, geralmente no contexto de lesões genitais/perineais extensas.
- Condiloma acuminado: é uma lesão de aspecto papilomatoso, com efeito citopático viral abundante, frequentemente associado com a presença de HPV DNA de baixo risco, como os subtipos 6 e 11.
- Carcinoma verrucoso: tem aspecto verrucoso, com atipia citológica discreta, consistindo em uma variante extremamente bem diferenciada do carcinoma espinocelular. Tradicionalmente, apresenta comportamento biológico destrutivo local, podendo metastatizar muito excepcionalmente. No ânus, as terminologias “condiloma gigante (maligno)” ou “tumor de Buschke-Löwenstein” são consideradas sinônimos de carcinoma verrucoso.
- Doença de Paget: a doença de Paget primária (extramamária) de região anal é rara, podendo estar associada ao adenocarcinoma de reto. Pode, ainda, estar associada à extensão da doença de Paget perineal, especialmente em mulheres no climatério.
- Carcinomas espinocelulares da pele perianal e borda anal são raros, representando cerca de 15% dos cânceres anais.
- Melanomas: na região anal, frequentemente são polipoides, podendo ser confundidos com hemorroidas e em até um terço dos casos sendo amelanóticos, o que dificulta o diagnóstico.
- Adenocarcinomas primários do canal anal são raros, podendo se originar em mucosa glandular e nas células mucossecretoras da região da linha pectínea ou do epitélio de revestimento dos ductos e glândulas anais; geralmente têm crescimento lento e se associam com fístulas e abscessos persistentes, no contexto da doença de Crohn, por exemplo.
VIII.2 Estudo imuno-histoquímico
Carcinomas espinocelulares de canal anal são mais frequentes, representando cerca de 75 a 80% dos tumores malignos anais. Embora representem neoplasias raras, há evidência de que sua incidência esteja aumentando, particularmente entre homens homossexuais, imunodeprimidos/suprimidos e mulheres com doença multifocal HPV induzida em trato anogenital inferior. O estudo imuno-histoquímico geralmente não é necessário para diagnóstico histológico, exceto nos casos em que, por causa da pouca diferenciação, é necessário o diagnóstico diferencial com carcinomas neuroendócrinos, melanoma e linfoma.
A realização de estudo imuno-histoquímico para p16 como marcador indireto de infecção por HPV de alto risco também pode ser útil.
VIII.3 Patologia molecular
O papel biológico crítico do papilomavírus humano (HPV) na carcinogênese das lesões anogenitais escamosas tem sido delineado há diversas décadas. A infecção por subtipo viral de baixo risco oncogênico (como os subtipos 6 e 11) usualmente cursa com uma infecção transitória, de morfologia tradicionalmente chamada displasia leve, grau 1 ou neoplasia intraepitelial de baixo grau. Já a infecção e a persistência da ação de um subtipo viral de alto risco oncogênico (dentre os quais se destacam os subtipos 16 e 18) podem gerar uma lesão pré-cancerosa, classicamente chamada de displasia moderada a acentuada ou neoplasia intraepitelial de alto grau. A identificação de DNA de HPV é de grande interesse em casos de carcinomas anais, posto que 90 a 93% dos carcinomas espinocelulares da região anal estão associados ao HPV, sobretudo os subtipos 16 e 18.
IX.Bibliografia
Amin MB, Edge SB, Greene FL, et al, eds. AJCC Cancer Staging Manual. 8th ed. New York, NY: Springer; 2017.
Benson III AB, Arnoletti JP, Bekai-Saab T, Chen YJ, Choti MA, Cooper HS et al. Anal carcinoma, version 2.2012: featured updates to the NCCN guidelines. NCCN guidelines Insights. JNCCN 2012; 10:449-54.
Bosman FT, Carneiro F, Hruban RH, Theise ND (eds.). WHO classification of tumors of the digestive system. 4. ed. Lyon: International Agency for Research on Cancer, 2010.
Darragh TM, Colgan TJ, Cox T, Heller DS, Henry MR, Luff RD et al.; members of Last Project Work Groups. The lower anogenital squamous terminology standardization project for HPV-associated lesions: background and consensus recommendations from the College of American Pathologists and the American Society for Colposcopy and Cervical Pathology. Arch Pathol Lab Med 2012; 136(10):1266-97.
Iacobuzio-Donahue CA, Montgomery E. Gastrointestinal and liver pathology. 2. ed. Philadelphia: Elsevier Saunders, 2012.
Kakar S, Shi C, Driman DK et al. members of the Cancer Committee, College of American Pathologists. Protocol for the examination of specimens from patients with carcinoma of the anus. version 4.0.1.0., 2017.
Odze RD, Goldblum JR. Surgical pathology of the GI tract, liver, biliary duct, and pancreas. 3. ed. Philadelphia: Elsevier Saunders, 2015.
Mills SE. Histology for pathologists. 4. ed. Philadelphia: Lippincott Williams & Wilkins, 2012.
Voltar para a página inicial do manual
